Distrofia di Fuchs, DSAEK e successivi interventi chirurgici: presentazione di due casi clinici
Abstract: Questo articolo analizza due casi clinici di pazienti affetti da distrofia di Fuchs seguiti presso la Clinica Oculistica di Sassari e dal Dottor Massimo D’Atri (direttore dell’UOC di Oculistica dell’Azienda Ospedaliera Brotzu di Cagliari), trattati con cheratoplastica endoteliale (DSAEK) e successivamente sottoposti ad un ulteriore trattamento chirurgico per altre patologie oculari. Prima di procedere al trattamento dei nostri pazienti abbiamo effettuato una ricerca per capire quale fosse il rischio. Abbiamo constatato che la letteratura scientifica non tratta di pazienti operati di DSAEK e successivamente sottoposti ad intervento chirurgico di vitrectomia per pucker maculare o ad impianto intravitreale di desametasone per edema maculare cistoide.
Keywords: distrofia di Fuchs, dsaek, edema maculare cistoide, pucker maculare, endotelio corneale, vitrectomia via pars plana, impianto intravitreale di desametasone, microscopia corneale confocale.
Introduzione
La distrofia corneale di Fuchs è la distrofia endoteliale corneale primaria più comune e rappresenta l'indicazione principale per il trapianto di cornea in tutto il mondo. È caratterizzata dal progressivo declino delle cellule endoteliali corneali e da alterazioni della matrice extracellulare della membrana di Descemet con la conseguente formazione di gutte che portano a edema corneale e riduzione dell’acuità visiva. La distrofia endoteliale corneale di Fuchs ha una maggiore incidenza nelle donne e si manifesta nella maggior parte dei casi nella quinta decade di vita.
La distrofia di Fuchs è una malattia genetica complessa ed eterogenea caratterizzata dall’interazione tra fattori genetici, epigenetici ed esogeni che portano ad un importante stress ossidativo, alla transizione endoteliale-mesenchimale, alla senescenza, alla disfunzione mitocondriale e infine all'apoptosi dell'endotelio corneale.
Tra le cause della distrofia di Fuchs ricordiamo la predisposizione genetica e i fattori ambientali quali i raggi UV (la maggior parte delle gutte si trova, infatti, in zona interpalpebrale), il fumo e un’alimentazione non corretta.
L'endotelio corneale è fondamentale per il mantenimento dell'equilibrio idrico e della trasparenza della cornea; è particolarmente suscettibile all'invecchiamento a causa del suo arresto post-mitotico, dell'elevata attività metabolica e dell'esposizione permanente alla luce ultravioletta.
Poiché l’endotelio ha una capacità replicativa minima in vivo e non è in grado di sostituire il proprio genoma, è particolarmente soggetto a danni cumulativi a carico del DNA acquisiti nel corso della vita. Nella distrofia di Fuchs i difetti genetici sottostanti rendono il genoma ancora più vulnerabile a questo danno, al punto da causare disfunzione mitocondriale, perdita di potenziale della membrana mitocondriale ed eccessiva attivazione della mitofagia. I fattori di stress intracellulari endogeni ed esogeni alterano l'impronta sintetica delle cellule, portando alla transizione endoteliale-mesenchimale e alla secrezione di matrice extracellulare aberrante con formazione di gutte e cicatrici. A loro volta le gutte o le cicatrici endoteliali contribuiscono al circolo vizioso della patogenesi della distrofia di Fuchs e, inducendo ulteriormente la transizione endotelio-mesenchimale e lo squilibrio ossidante-antiossidante, perpetuano i cambiamenti molecolari dell’endotelio degenerato.
La distrofia endoteliale corneale di Fuchs è stata descritta per la prima volta circa un secolo fa. Da allora sono stati fatti numerosi passi avanti sulle manifestazioni cliniche, sul trattamento chirurgico e non chirurgico, sull'aspetto microscopico e sulla patogenesi. Negli ultimi dieci anni sono stati compiuti progressi significativi per quanto riguarda la patogenesi genetica della distrofia di Fuchs. Una forma rara e ad esordio precoce della malattia è stata attribuita a mutazioni missenso nel gene COL8A2, mentre la stragrande maggioranza dei casi ad esordio tardivo può essere attribuita a un'espansione ripetuta non codificante all'interno del gene TCF4.
Nel Regno Unito la raccomandazione è di analizzare il materiale corneale rimosso e sottoporlo ad analisi istologica.
Negli Stati Uniti la cheratoplastica endoteliale è diventata il trattamento di prima scelta per la distrofia endoteliale di Fuchs e rappresenta l’indicazione più frequente alla cheratoplastica endoteliale (DSAEK). Nella DSAEK la membrana di Descemet e l’endotelio sono rimossi dal donatore e impiantati nel paziente ricevente con una variabilità nello spessore dello stroma del donatore. La funzione visiva e la qualità della vita migliorano rapidamente dopo la DSAEK e la sopravvivenza a cinque anni dal trapianto è paragonabile a quella dopo cheratoplastica perforante.
La distrofia endoteliale di Fuchs è tipicamente una malattia ad esordio tardivo caratterizzata da una degenerazione lenta e progressiva.
All’esordio i pazienti sono generalmente asintomatici. Con il progredire della patologia al mattino compaiono i primi sintomi caratterizzati dalla visione di aloni, secondari all'aumento dell'edema corneale dopo la notte. Nelle fasi più avanzate i sintomi come diminuzione della vista, fotofobia, epifora e dolore sono presenti tutto il giorno in quanto vi è un aumento dell’edema con rottura delle bolle epiteliali, che può portare ad un difetto epiteliale persistente o ad un’ulcera corneale.
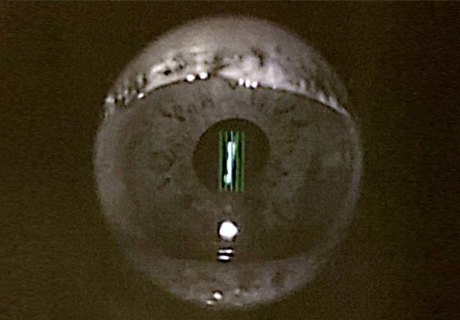
L'esame della cornea con il biomicroscopio con lampada a fessura consente l'esame diretto (illuminazione diffusa, illuminazione focale e riflessione speculare) e indiretta (illuminazione prossimale, diffusione sclerotica e retroilluminazione) dei diversi strati della cornea.
L'illuminazione a fessura con un fascio sottile consente la visualizzazione dell’endotelio corneale e di eventuali anomalie, incluse bolle epiteliali, edema corneale e gutte.
L’analisi fotografica con retroilluminazione, con conteggio manuale o automatizzato delle gutte, si è dimostrata un modo efficace per documentare il numero e la distribuzione delle gutte, per dimostrare la formazione di nuove gutte e la loro progressione nel tempo.
La stadiazione della distrofia di Fuchs può essere valutata mediante la scala di Krachmer mediante biomicroscopia con lampada a fessura, valutando la confluenza e l'area delle gutte, la presenza di edema stromale o epiteliale corneale.
La scala di Krachmer comprende 6 stadi dove i non affetti sono stati classificati 0, i casi intermedi sono stati classificati da 1 a 3 e i casi gravi sono stati classificati da 4 a 6. Questo è un sistema semplice di classificazione per la valutazione della gravità della patologia.
La diagnosi di distrofia di Fuchs viene effettuata attraverso un’accurata visita oculistica, la misurazione dello spessore corneale e l'analisi delle cellule endoteliali corneali.
Alcuni accorgimenti diagnostici importanti in un paziente con distrofia di Fuchs sono:
- valutazione del numero delle cellule endoteliali sia in zona ottica che in zona periferica;
- valutazione dello spessore corneale e del mosaico endoteliale;
- valutazione di ulteriori fattori: CV (indice variazione cellulare <=32%), HEX (indice di esagonalità)
